在實驗室中,若要證明某一混合氣體(以下簡稱氣體a)中含有二氧化碳、一氧化碳和水蒸氣,需要設計一套系統、嚴謹且邏輯順序合理的實驗流程。由于水蒸氣、二氧化碳和一氧化碳的化學性質不同,且驗證過程可能相互干擾,因此操作順序至關重要。通常遵循“先驗水、后驗其它,排除干擾”的原則。
核心原則與注意事項
1. 驗證順序:必須先驗證水蒸氣的存在,因為后續驗證二氧化碳和氧化碳的試劑(如無水硫酸銅、澄清石灰水、濃硫酸等)通常是水溶液或具有吸水性,會引入或吸收水汽,干擾水蒸氣的鑒定。
2. 氣體凈化與干燥:在驗證水蒸氣后,需將氣體充分干燥(如通過濃硫酸或無水氯化鈣),再進行后續檢驗,以避免水蒸氣對二氧化碳檢驗的潛在影響(雖然影響較小,但嚴謹實驗要求)。
3. 一氧化碳的驗證:一氧化碳的驗證通常涉及其還原性,需要通過轉化反應(如還原氧化銅生成二氧化碳)進行間接證明,因此需要安排在二氧化碳驗證之后,并對新生成的二氧化碳進行二次驗證。
4. 尾氣處理:一氧化碳有毒,實驗必須設計尾氣處理裝置(如點燃或收集),確保安全。
假設實驗室提供的儀器與藥品可能包括:
- 氣體發生裝置(或氣體a的儲存裝置,如儲氣袋)
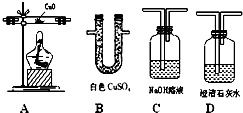
- 干燥管、U型管、洗氣瓶、硬質玻璃管、酒精燈(或酒精噴燈)、導管等。
- 藥品:無水硫酸銅(白色)、澄清石灰水、濃硫酸、新鮮的氧化銅粉末(黑色)、氫氧化鈉溶液、氣球或尾氣處理裝置等。
推薦實驗步驟與裝置連接順序:
第一步:驗證水蒸氣(H?O)的存在
1. 將氣體a通入盛有無水硫酸銅的干燥管或U型管中。
2. 現象與結論:若白色無水硫酸銅粉末變為藍色,則證明混合氣體中含有水蒸氣。
第二步:除去水蒸氣并驗證二氧化碳(CO?)的存在
1. 將經過第一步驗證后的氣體(或直接從氣源引出,但已確知含水)通入盛有濃硫酸的洗氣瓶,以完全除去水蒸氣。
2. 將干燥后的氣體通入盛有澄清石灰水的洗氣瓶或試管中。
3. 現象與結論:若澄清石灰水變渾濁,則證明原混合氣體中含有二氧化碳。
第三步:除去二氧化碳,為驗證一氧化碳做準備
1. 將氣體通入盛有足量氫氧化鈉溶液(或堿石灰)的洗氣瓶或U型管中,以徹底除去二氧化碳,防止其干擾后續對一氧化碳的檢驗。
2. 可選步驟:為確保二氧化碳除盡,可再將氣體通入一次澄清石灰水,確認不再變渾濁。
第四步:驗證一氧化碳(CO)的存在
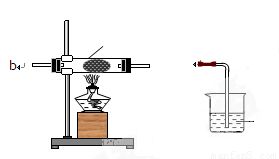
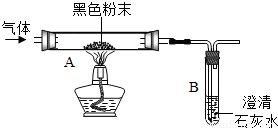
1. 將除去水和二氧化碳的氣體通入盛有新鮮黑色氧化銅粉末的硬質玻璃管,并加熱(用酒精燈或酒精噴燈)。
2. 現象與結論:
- 硬質玻璃管中的黑色氧化銅固體逐漸變為光亮的紅色(生成銅)。
- 將反應后產生的氣體再次通入另一份新鮮的澄清石灰水中。
- 若該澄清石灰水變渾濁,則證明有二氧化碳生成。結合氧化銅被還原為銅的現象,即可推斷原混合氣體中含有一氧化碳(因其具有還原性,并與氧化銅反應生成了二氧化碳)。
第五步:尾氣處理
由于從氧化銅管出來的氣體可能含有未反應完的一氧化碳,必須進行處理。可在最后導氣管口點燃(確保氣體已純凈,防止爆炸)或用氣球收集,以防污染空氣。
實驗裝置連接總順序示意圖(氣流方向從左至右):
氣體a發生/儲存裝置 → 無水硫酸銅(驗水) → 濃硫酸(干燥) → 澄清石灰水(驗CO?) → 氫氧化鈉溶液(除CO?) → 干燥管(可選,進一步干燥) → 加熱的氧化銅 → 澄清石灰水(驗新生成CO?) → 尾氣處理裝置。
結論:通過以上順序操作,觀察到的系列現象——無水硫酸銅變藍、第一次澄清石灰水變渾濁、氧化銅由黑變紅且第二次澄清石灰水變渾濁——能夠形成完整的證據鏈,嚴謹地證明混合氣體a中同時含有水蒸氣、二氧化碳和一氧化碳三種組分。